Ciri-ciri Fizikal Air & Teori Kinetik
Takat beku air
Takat beku air (freezing point of water) adalah suhu di mana air bertukar menjadi ais (bentuk pepejal).
Takat beku air tulen (pure water) pada tekanan atmosfera (piawai) ialah 0°C. Ini bermakna bahawa air tulen akan membeku menjadi ais (ice) pada 0°C.
Takat didih air
Takat didih air (boiling point of water) ialah suhu di mana air bertukar menjadi stim (wap air).
Takat didih air pada suhu bilik dan tekanan atmosfera (piawai) adalah 100°C. Oleh itu, air akan mendidih dan bertukar menjadi stim (steam) pada suhu 100°C.
Teori Kinetik
Teori Kinetik adalah penjelasan tentang keadaan zarah-zarah (particles) dalam jirim.
Terdapat tiga andaian yang dibuat dalam teori kinetik:
- Semua jirim (matter) terdiri terdiri daripada zarah-zarah kecil / seni (seperti atom dan molekul).
- Zarah-zarah ini adalah sentiasa bergerak / bergetar, secara rawak.
- Zarah-zarah ini juga berlanggar (colliding) antara satu sama lain.
Molekul mempunyai pergerakan dan tenaga kinetik pada semua suhu. Molekul
air beku (ice) pada 0°C bergerak lebih perlahan daripada molekul air
pada 10°C.
Perubahan keadaan jirim boleh ditafsirkan melalui teori kinetik jirim (kinetic theory of matter).
Pembekuan
Apabila cecair disejukkan, pergerakan zarah akan menjadi perlahan. Oleh itu, tenaga kinetik zarah berkurang.
Daya tarikan antara zarah menjadi lebih kuat dan kukuh.
Apabila daya tarikan (daya yang menarik) menjadi begitu kuat, ianya
menarik zarah kembali ke kedudukan tetap mereka, cecair menjadi pepejal.
Perubahan dalam susunan dan gerakan zarah ini dipanggil pembekuan (freezing).
Suhu dimana cecair (liquid) berubah menjadi pepejal dipanggil takat beku (0°C).
Pendidihan
Apabila cecair dipanaskan, zarah akan bergetar dengan lebih pantas. Oleh itu, tenaga kinetik zarah meningkat.
Zarah akan bergerak menjauhi satu sama lain dan daya tarikan antara mereka menjadi lemah (weaken).
Apabila kumpulan kecil zarah-zarah dipecahkan kepada zarah tunggal dan
daya tarikan antara zarah boleh diabaikan (negligible), cecair bertukar
menjadi gas.
Perubahan dalam susunan dan gerakan zarah ini dipanggil pendidihan (boiling).
Suhu dimana cecair bertukar menjadi gas (atau dalam bentuk buih pada seluruh cecair), dipanggil takat didih (100°C).
Air wujud dalam keadaan pepejal, cecair dan gas. Berdasarkan Teori Kinetik Jirim, air terdiri daripada partikel sangat kecil dan tersusun dan bergerak mengikut keadaannya yang tertentu. Bermaksud, pada keadaan pepejal, susunan dan pergerakan molekul air adalah tidak sama seperti pada keadaan cecair.
Takat beku air
- Takat beku air adalah suhu di mana air berubah daripada cecair kepada pepejal.
- Takat beku air = 0 C
Takat didih air
- Takat didih air adalah suhu di mana air berubah daripada cecair kepada gas.
- Takat didih air = 100 C
Air ialah sebatian yang terdiri daripada oksigen dan hidrogen. Bagi setiap 1 molekul air, ada 2 atom hidrogen yang telah bergabung dengan 1 atom oksigen. Komposisi air atau kandungan air ini boleh diuraikan semula kepada bahan asas nya melalui proses elektrolisis. Elektrolisis adalah proses menguraikan elektrolit (dalam kes ini adalah air) kepada komponen asalnya, iaitu oksigen dan hidrogen.

Komposisi 1 molekul air yang terbentuk daripada gabungan 1 atom oksigen dan 2 atom hidrogen.
Elektrolisis adalah proses menguraikan elektrolit (dalam kes ini adalah air) kepada komponen asalnya, iaitu oksigen dan hidrogen.
penyejatan air
Penyejatan adalah proses perubahan cecair menjadi gas pada sebarang suhu di bawah takat didih cecair itu. Kadar penyejatan bergantung kepada beberapa faktor persekitaran seperti kelembapan udara, suhu sekeliling, luas permukaan dan pergerakan udara.
Faktor Yang Mempengaruhi Penyejatan Air
1) Kelembapan
Jika kelembapan tinggi, kadar penyejatan rendah (sebab banyak kandungan air dalam udara)
Jika kelembapan rendah, kadar penyejatan tinggi (sebab sedikit kandungan air dalam udara membolehkan penyejatan berlaku dengan lebih cepat)
2) Suhu Sekeliling
Jika suhu rendah, kadar penyejatan rendah (sebab molekul bergerak perlahan)
Jika suhu tinggi, kadar penyejatan tinggi (sebab molekul bergerak pantas)
3) Luas Permukaan
Jika luas permukaan kecil, kadar penyejatan rendah (sebab ruang yang kecil membataskan air untuk tersejat dengan bebas)
Jika luas permukaan besar, kadar penyejatan tinggi (sebab ruang yang besar membenarkan berlakunya penyejatan dengan lebih banyak)
4) Pergerakan Udara
Jika udara tenang, kadar penyejatan rendah (sebab molekul air terkumpul di permukaan air)
Jika udara bergerak, kadar penyejatan tinggi (sebab molekul air yang tersejat akan tersebar dengan cepat ke persekitaran serta membolehkan penyejatan berlaku lagi)
Persamaan dan Perbezaan Antara Penyejatan dan Pendidihan
Persamaan
1) berubah daripada cecair kepada gas
2) menyerap haba
Perbezaan
1) Suhu
Penyejatan berlaku pada sebarang suhu bawah takat didih
Pendidihan berlaku pada takat didih (100 C)
2) Kawasan
Penyejatan berlaku pada permukaan sahaja
Pendidihan berlaku pada seluruh bahagian cecair
3) Kehadiran Gelembung Gas
Penyejatan tidak membentuk gelembung gas
Pendidihan membentuk gelembung gas
4) Haba
Penyejatan menyerap haba daripada persekitaran
Pendidihan menyerap haba daripada sumber pemanasan (api)
5) Kelajuan Proses
Penyejatan merupakan proses yang lambat
Pendidihan merupakan proses yang cepat
Aplikasi Proses Penyejatan Dalam Kehidupan Seharian
1) Mengeringkan Pakaian
2) Pengawetan hasil pertanian
3) Pemprosesan makanan
larutan dan keterlarutan
Bagi menganalisa larutan, anda perlu tahu apa itu pelarut dan zat terlarut. Jom kita tengok apa definisi dan contoh bagi istilah yang telah dinyatakan tadi.
Larutan
Larutan adalah hasil campuran yang terbentuk apabila zat terlarut melarut dalam pelarut
eg : Larutan gula
Zat Terlarut
Zat Terlarut adalah bahan yang boleh melarut dalam cecair
eg : Gula
Pelarut
Pelarut adalah cecair yang boleh melarutkan bahan
eg : Air
Larutan Cair, Larutan Pekat dan Larutan Tepu
Air adalah pelarut universal yang dapat melarutkan banyak bahan. Walaubagaimanapun, isipadu air yang tertentu hanya dapat melarutkan zat terlarut dalam kuantiti yang terhad.
Larutan Cair
Kandungan zat terlarut yang sedikit dalam pelarut
Larutan Pekat
Kandungan zat terlarut yang banyak dalam pelarut
Larutan Tepu
Kandungan zat terlarut yang berlebihan dalam pelarut
Keterlarutan
Keterlarutan memberi maksud kuantiti maksimum bagi sesuatu bahan yang dapat dilarutkan dalam pelarut pada suhu yang tertentu. Faktor yang mempengaruhi kadar keterlarutan adalah suhu pelarut, kadar kacauan dan saiz zat terlarut.
1) Suhu Pelarut
Semakin tinggi suhu pelarut, maka kadar keterlarutan adalah lebih tinggi
kerana lebih banyak zat terlarut yang boleh larut pada suhu lebih tinggi
2) Kadar Kacauan
Semakin tinggi kadar kacauan, maka kadar keterlarutan adalah lebih tinggi
kerana proses mengacau dapat mempercepatkan lagi kadar melarut
3) Saiz Zat Terlarut
Semakin kecil saiz zat terlarut, maka kadar keterlarutan adalah lebih tinggi
lebih cepat melarut kerana luas permukaan yang lebih besar
asid dan alkali
sid dan alkali banyak digunakan dalam kehidupan seharian kita. Kadang-kadang kita memasak menggunakan cuka, iaitu bahan berasid. Mencuci pakaian dengan menggunakan sabun pencuci atau detergen yang beralkali. Jom kita tengok perbezaan dan persamaan sifat bagi asid dan alkali. Harus diingat, asid dan alkali hanya boleh menunjukkan ciri-ciri mereka jika berada di dalam air!

Perbandingan Sifat Asid dan Alkali
Persamaan
1) Kedua-duanya larut dalam air
2) Bersifat mengakis jika pekat
Perbezaan
1) Rasa
Asid rasa masam, Alkali rasa pahit
2) Kertas Litmus
Asid menukarkan kertas litmus biru kepada merah, Alkali menukarkan kertas litmus merah kepada biru
3) Nilai pH
Asid kurang daripada 7, Alkali lebih daripada 7
4) Tindakbalas dengan logam
Asid menghasilkan gas hidrogen, Alkali tidak ada tindakbalas
Peneutralan
Peneutralan adalah tindakbalas antara asid dan alkali yang menghasilkan garam dan air.
asid + alkali -> garam + air
Aplikasi Peneutralan Dalam Kehidupan Seharian
1) Ubat Gigi - Mencegah kerosakan gigi
Ubat gigi (alkali) meneutralkan asid yang dihasilkan oleh bakteria dalam mulut
2) Syampu dan perapi - Menjaga kesihatan rambut
Syampu (alkali) perlu digunakan bersama Perapi (asid) untuk penjagaan rambut
3) Sengatan serangga
Sengatan lebah (asid) dirawat dengan losyen kalamina (alkali)
Sengatan tebuan (alkali) dirawat dengan asid cair
4) Ubat Pencernaan - Merawat gastrik
Gastrik (asid) dirawat dengan susu magnesia (alkali)
pembersihan air
da beberapa kaedah pembersihan air, antaranya pendidihan, pengklorinan, penurasan dan penyulingan. Masing-masing mempunyai kelebihan dan kekurangan masing-masing. Air yang datang daripada sumber yang kita gunakan, sama ada dari paip atau pun dari sumber sungai dan lain-lain, merupakan air yang masih perlu dirawat. Air mentah dari pelbagai sumber ini perlulah menjalani kaedah pembersihan air sebelum selamat untuk digunakan.
a) Penurasan
Kaedah penurasan menggunakan beberapa lapisan bahan (batuan, pasir) sebagai penapis semulajadi kepada air yang mahu dibersihkan tersebut.
Kebaikan : Air jernih dan bebas daripada zarah terampai
Keburukan : Air masih mengandungi mikroorganisma dan bahan terlarut
b) Pendidihan
Pendidihan dilakukan dengan cara memanaskan air sehingga mendidih, iaitu sehingga mencapai takat didih, 100 C.
Kebaikan : Air bebas daripada mikroorganisma hidup
Keburukan : Air masih mengandungi zarah terampai dan bahan terlarut
c) Pengklorinan
Pengklorinan adalah cara membersihkan air dengan cara menambahkan klorin ke dalam air tersebut bagi tujuan untuk membunuh mikroorganisma
Kebaikan : Air bebas daripada mikroorganisma hidup
Keburukan : Air masih mengandungi zarah terampai dan bahan terlarut
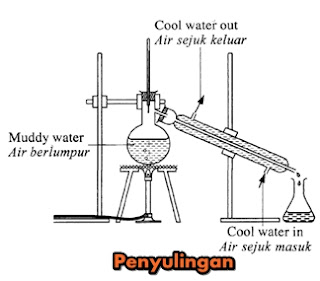
d) Penyulingan
Penyulingan adalah melalui proses dalam makmal dengan radas yang disediakan seperti di bawah dan menggunakan konsep kondensasi gas kepada cecair bagi menulenkan air yang kotor.
Kebaikan : Air bebas daripada mikroorganisma, zarah terampai dan bahan terlarut
Keburukan : Tidak mengandungi zat mineral yang berguna kepada kesihatan badan
sistem bekalan air
Di Malaysia, bekalan air bersih adalah berasal daripada air hujan yang terkumpul di sungai dan mengalir ke empangan. Bekalan air kepada pengguna adalah melalui satu sistem rangkaian saluran paip yang membawa air dari loji pembersihan air. Dalam sistem bekalan air, air yang dirawat harus melalui 6 fasa pembersihan sebelum dapat diedarkan kepada pengguna.

1) Penapisan
Menyingkirkan bahan pepejal yang kasar seperti daun dan ranting
2) Pengoksidaan
Oksigen dilarutkan dalam air untuk menyingkirkan bau busuk
3) Penggumpalan
Alum ditambah untuk membentuk bahan mendak yang kasar
Kapur terhidrat ditambah bagi merendahkan keasidan air
4) Pengenapan
Mendakan, bakteria dan kotoran terampai tenggelam ke dasar tangki
5) Penurasan
Air dialirkan melalui lapisan pasir untuk menyingkirkan bahan pepejal yang lain
6) Pengklorinan dan Pengfluoridaan
Klorin dapat membunuh mikroorganisma.
Fluorida dapat mengurangkan pereputan gigi
pemeliharaan kualiti air
Pemeliharaan kualiti air selalunya dikaitkan dengan pencemaran air dan jenis-jenis bahan buangan yang mencemarkan air. Justeru itu, kita sebagai pengguna perlulah menggunakan air dengan bijak dan melakukan perkara-perkara yang sekurang-kurang nya boleh membantu mengurangkan pencemaran air.
Jenis-jenis Bahan Yang Menyebabkan Pencemaran Air
1) Bahan buangan industri
Sumber : Kilang industri
Kandungan : Ianya mengandungi sisa kimia atau sisa radioaktif
Kesan : Menjejaskan hidupan akuatik dan manusia yang memakan hidupan tersebut
2) Bahan buangan domestik
Sumber : Kediaman
Kandungan : Sampah sarap dan air kumbahan
Kesan : Menghalang aliran air sungai, Kekurangan oksigen terlarut dalam air
3) Bahan kimia pertanian
Sumber : Ladang pertanian dan sawah padi
Kandungan : Baja kimia dan pestisid
Kesan : Pertumbuhan alga yang menjejaskan hidupan akuatik lain
4) Pengelodakan sungai
Sumber : Pembangunan dan penebangan hutan
Kandungan : Lumpur dan kelodak
Kesan : Mengakibatkan banjir kilat, Sungai semakin cetek
5) Tumpahan minyak
Sumber : Kapal tangki minyak
Kandungan : Minyak
Kesan : Menjejaskan hidupan akuatik dan burung di kawasan laut berkenaan
Cara-cara Mengawal Pencemaran Air
1) Bahan buangan dan sisa kimia tidak boleh dibuang ke dalam sungai
2) Sampah dilupuskan secara sistematik oleh pihak pelupusan sampah
3) Bahan beracun dari kilang hendaklah ditapis atau dirawat sebelum disalurkan ke sungai
4) Penjualan pestisid diperketatkan
5) Bahan bukan organik hendaklah dikitar semula
6) Mempergiatkan usaha mendapatkan tenaga biojisim daripada sampah sarap












Terima kasih :)
ReplyDeleteterima kasih .)
ReplyDelete.)
nk tye.. bendasing tu ape? Bahan terlarut ke apa?
ReplyDeleteThis comment has been removed by the author.
Deleteada pencemaran sungao tak??
ReplyDeletethank :)
ReplyDeletetq
ReplyDeleteWaw
ReplyDeleteWaw
ReplyDeleteWaw
ReplyDeletetq
ReplyDeleteTq
ReplyDelete104 panjangnya cuti ku sebelum cuti ku sekolah bermula🤪#phineas and ferb
ReplyDeleteTq
ReplyDeletetq
ReplyDeletetq...harap2 corona ni cepat hilang...susah nak belajar dirumah
ReplyDeleteBetul...Ye
DeleteSaya nak perbezaan kadar antara penyejatan dan pendidihan...
ReplyDeleteKepentingan penyejatan air kepada badan manusia
ReplyDeletetq :)
ReplyDeleteGood🤧tq:3
ReplyDeleteApakah bentuk jirim bagi larutan gula?
ReplyDeleteair laut or air suling yg lg cpt didih
ReplyDeleteAir sungai....heheh...air suling
Delete